Våra huvudprodukter: Aminosilikon, blocksilikon, hydrofil silikon, alla deras silikonemulsioner, vätförbättrare för friktionsbeständighet, vattenavvisande medel (fluorfri, kol 6, kol 8), demineraliseringskemikalier (ABS, enzym, spandexskydd, manganborttagare). För mer information, kontakta: Mandy +86 19856618619 (Whatsapp)
Introduktion till tensider
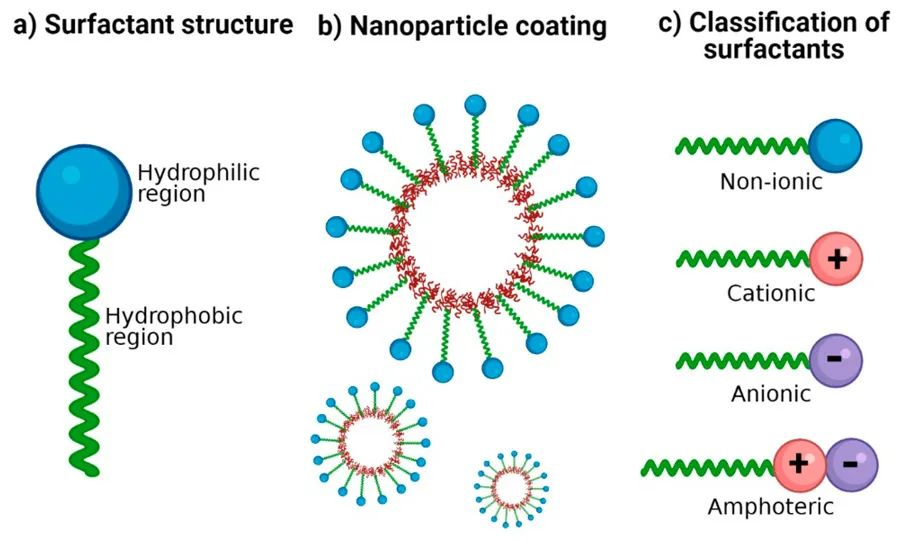
Tensider har en amfifil molekylstruktur: ena änden innehåller en hydrofil grupp, kallad det hydrofila huvudet, medan den andra änden innehåller en hydrofob grupp, känd som den hydrofoba svansen. Det hydrofila huvudet gör att tensider kan lösas upp i vatten i sin monomerform.
Den hydrofila gruppen är ofta en polär grupp, som kan vara en karboxylgrupp (-COOH), en sulfonsyragrupp (-SO3H), en aminogrupp (-NH2), aminer och deras salter, hydroxylgrupper (-OH), amidgrupper eller eterbindningar (-O-) som andra exempel på polära hydrofila grupper.
Den hydrofoba gruppen är vanligtvis en opolär kolvätekedja, såsom hydrofoba alkylkedjor (R- för alkyl) eller aromatiska grupper (Ar- för aryl).
Tensider kan kategoriseras i joniska tensider (inklusive katjoniska och anjoniska tensider), nonjoniska tensider, amfotära tensider, blandade tensider och andra. I tensidlösningar, när koncentrationen av tensid når ett visst värde, kommer tensidmolekyler att bilda olika ordnade aggregat som kallas miceller. Micelliseringsprocessen, eller micellbildning, är en avgörande grundläggande egenskap hos tensidlösningar, eftersom många viktiga gränsytfenomen är förknippade med bildandet av miceller.
Koncentrationen vid vilken tensider bildar miceller i lösning kallas kritisk micellkoncentration (CMC). Miceller är inte fixerade, sfäriska strukturer; snarare uppvisar de extrem oregelbundenhet och dynamiska formförändringar. Under vissa förhållanden kan tensider också uppvisa omvända micelltillstånd.
Faktorer som påverkar CMC:
- Strukturen hos det ytaktiva medlet
- Typ och förekomst av tillsatser
- Temperatur
Interaktioner mellan tensider och proteiner
Proteiner innehåller opolära, polära och laddade grupper, och många amfifila molekyler kan interagera med proteiner på olika sätt. Beroende på förhållandena kan tensider bilda molekylärt organiserade aggregat med olika strukturer, såsom miceller eller omvända miceller, vilka interagerar olika med proteiner.
Interaktionerna mellan proteiner och tensider (protein-surfaktant, PS) involverar främst elektrostatiska interaktioner och hydrofoba interaktioner. Joniska tensider interagerar med proteiner huvudsakligen genom de elektrostatiska krafterna hos den polära gruppen och de hydrofoba interaktionerna hos den alifatiska kolkedjan, och binder till proteinets polära och hydrofoba regioner och bildar därmed PS-komplex.
Nonjoniska tensider interagerar primärt med proteiner genom hydrofoba krafter, där de hydrofoba kedjorna interagerar med proteinernas hydrofoba regioner. Interaktionen kan påverka både strukturen och funktionen hos det ytaktiva medlet och proteinet. Därför avgör typen och koncentrationen av tensider, tillsammans med miljökontexten, huruvida tensider stabiliserar eller destabiliserar proteiner, samt om de främjar aggregering eller dispersion.
HLB-värde för tensider
För att ett tensid ska uppvisa sin unika gränsytaktivitet måste det balansera de hydrofoba och hydrofila komponenterna. HLB (hydrofil-lipofilbalans) är ett mått på den hydrofila-lipofila balansen hos tensider och fungerar som en indikator på tensidernas hydrofila och hydrofoba egenskaper.
HLB-värdet är ett relativt värde (från 0 till 40). Till exempel har paraffin ett HLB-värde på 0 (ingen hydrofil komponent), polyetylenglykol har ett HLB-värde på 20 och det mycket hydrofila SDS (natriumdodecylsulfat) har ett HLB-värde på 40. HLB-värdet kan fungera som en vägledande referens vid val av tensider. Ett högre HLB-värde indikerar bättre hydrofilicitet, medan ett lägre HLB-värde tyder på sämre hydrofilicitet.
Publiceringstid: 10 sep-2024

