

Krympkraften för varje enhetslängd på vätskans yta kallas ytspänningen, och enheten är N. · m-1.

Egenskapen att minska ytspänningen hos lösningsmedlet kallas ytaktivitet, och ett ämne med denna egenskap kallas en ytaktiv substans.
Den ytaktiva substansen som kan binda molekyler i vattenlösning och bilda miceller och andra föreningar och ha hög ytaktivitet, samtidigt som det har effekten av vätning, emulgering, skumning, tvätt, etc. kallas ytaktiva medel.
Surfaktant är organiska föreningar med speciell struktur och egenskaper, vilket kan förändra gränsytespänningen avsevärt mellan två faser eller ytspänningen hos vätskor (vanligtvis vatten), med vätning, skumning, emulgering, tvätt och andra egenskaper.
När det gäller struktur har ytaktiva medel ett gemensamt drag genom att de innehåller två grupper av olika natur i sina molekyler. I ena änden är en lång kedja av icke-polär grupp, löslig i olja och olöslig i vatten, även känd som hydrofob grupp eller vattenavvisande grupp. En sådan vattenavvisande grupp är i allmänhet långa kedjor av kolväten, ibland också för organisk fluor, kisel, organofosfat, organotinkedja, etc. I andra änden är vattenlöslig grupp, en hydrofil grupp eller oljeavvisande grupp. Den hydrofila gruppen måste vara tillräckligt hydrofil för att säkerställa att hela ytaktiva medel är lösliga i vatten och har den nödvändiga lösligheten. Eftersom ytaktiva medel innehåller hydrofila och hydrofoba grupper kan de vara lösliga i minst en av de flytande faserna. Denna hydrofila och lipofil egenskap hos ytaktivt medel kallas amfifilicitet.


Surfaktant är ett slags amfifila molekyler med både hydrofoba och hydrofila grupper. Hydrofoba grupper av ytaktiva ämnen består vanligtvis av långkedjiga kolväten, såsom rak kedjan alkyl C8 ~ C20, grenad kedjan alkyl C8 ~ C20 , alkylfenyl (alkylkolomnummer är 8 ~ 16) och liknande. Skillnaden som är liten mellan hydrofoba grupper är främst i de strukturella förändringarna av kolvätekedjor. Och de typer av hydrofila grupper är mer, så egenskaperna hos ytaktiva medel är huvudsakligen relaterade till hydrofila grupper utöver storleken och formen hos hydrofoba grupper. De strukturella förändringarna av hydrofila grupper är större än de hos hydrofoba grupper, så klassificeringen av ytaktiva medel är vanligtvis baserade på strukturen hos hydrofila grupper. Denna klassificering är baserad på om den hydrofila gruppen är jonisk eller inte, och den är uppdelad i anjoniska, katjoniska, nonjoniska, zwitterioniska och andra speciella typer av ytaktiva medel.

① Adsorption av ytaktiva medel vid interfac
Surfaktiva molekyler är amfifila molekyler med både lipofila och hydrofila grupper. När det ytaktiva ämnet upplöses i vatten, lockas dess hydrofila grupp av vatten och upplöses i vatten, medan dess lipofila grupp avvisas av vatten och lämnar vatten, vilket resulterar i adsorption av ytaktiva molekyler (eller joner) på gränssnittet mellan de två faserna, vilket minskar interfasen mellan de två faserna. Ju mer ytaktiva molekyler (eller joner) adsorberas vid gränssnittet, desto större minskning av gränsytespänningen.
② Några egenskaper hos adsorptionsmembran
Yttrycket av adsorptionsmembran: ytaktivt adsorption vid gas-vätskan för att bilda ett adsorptionsmembran, såsom placera ett friktionslöst avtagbart flytande ark på gränssnittet, vilket flytande ark trycker adsorbentmembranet längs lösningsytan, och membranet genererar ett tryck på flytande ark, vilket kallas yttrycket.
Ytviskositet: Liksom yttryck är ytviskositet en egenskap som uppvisas av olösligt molekylmembran. Suspenderad av en fin metalltrådplatinring, så att dess plan kontaktar tankens vattenyta, roterar platinringen, platinringen med viskositeten hos vattenhindret, amplituden gradvis förfaller, enligt vilken ytviskositeten kan mätas. Metoden är: Först genomförs experimentet på den rena vattenytan för att mäta amplitudförfallet, och sedan mäts förfallet efter bildandet av ytmembranet och viskositeten hos ytmembranet härrör från skillnaden mellan de två.
Ytviskositeten är nära besläktad med ytmembranets soliditet, och eftersom adsorptionsmembranet har yttryck och viskositet måste det ha elasticitet. Ju högre yttrycket och desto högre viskositet hos det adsorberade membranet, desto högre är dess elastiska modul. Den elastiska modulen för ytadsorptionsmembranet är viktigt i processen med bubbelstabilisering.
③ Bildning av miceller
Utspädda lösningar av ytaktiva medel följer lagarna följt av ideala lösningar. Mängden ytaktiva adsorberade på ytan av lösningen ökar med koncentrationen av lösningen, och när koncentrationen når eller överskrider ett visst värde, ökar inte längre mängden adsorption. Både praxis och teori visar att de bildar föreningar i lösning, och dessa föreningar kallas miceller.
Kritisk micellkoncentration (CMC): Den minsta koncentrationen vid vilken ytaktiva medel bildar miceller i lösning kallas den kritiska micellkoncentrationen.
④ CMC -värden för vanliga ytaktiva ämnen.

HLB är förkortningen av hydrofil lipofilbalans, vilket indikerar den hydrofila och lipofila balansen hos de hydrofila och lipofila grupperna i det ytaktiva ämnet, dvs HLB -värdet för det ytaktiva ämnet. Ett stort HLB -värde indikerar en molekyl med stark hydrofilicitet och svag lipofilicitet; Omvänt, stark lipofilicitet och svag hydrofilicitet.
① Bestämmelser i HLB -värde
HLB-värdet är ett relativt värde, så när HLB-värdet utvecklas, som ett standard, är HLB-värdet för paraffinvax, som inte har några hydrofila egenskaper, därför är HLB-värdet för surfaktanter i allmänhet att vara mer än 40. 10 är lipofila, medan de större än 10 är hydrofila. Således är vändpunkten från lipofil till hydrofila cirka 10.
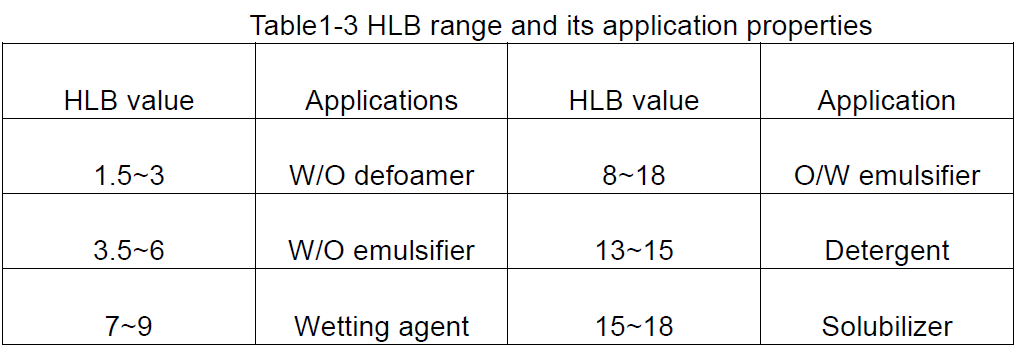
Baserat på HLB-värdena för ytaktiva ämnen kan en allmän uppfattning om deras möjliga användningar erhållas, såsom visas i tabell 1-3.

Två ömsesidigt olösliga vätskor, en spridd i den andra som partiklar (droppar eller flytande kristaller) bildar ett system som kallas en emulsion. Detta system är termodynamiskt instabilt på grund av ökningen i gränsområdet för de två vätskorna när emulsionen bildas. För att göra emulsionen stabil är det nödvändigt att lägga till en tredje komponent - emulgator för att minska systemets gränsytanergi. Emulgeringare tillhör ytaktivt medel, dess huvudfunktion är att spela rollen som emulsion. Fasen för emulsionen som finns som droppar kallas den spridda fasen (eller inre fasen, diskontinuerlig fas), och den andra fasen som är kopplad samman kallas dispersionsmediet (eller yttre fas, kontinuerlig fas).
① Emulgiatorer och emulsioner
Common emulsions, one phase is water or aqueous solution, the other phase is organic substances not miscible with water, such as grease, wax, etc. The emulsion formed by water and oil can be divided into two types according to their dispersion situation: oil dispersed in water to form oil-in-water type emulsion, expressed as O/W (oil/water): water dispersed in oil to form oil-in-water type emulsion, expressed as W/O (vatten/olja). Komplexa vatten-i-olja-i-vatten w/o/W-typ och olja-i-vatten-i-olja O/W/O-typ multiemulsioner kan också bildas.
Emulgiatorer används för att stabilisera emulsioner genom att minska gränsytespänningen och bilda en-molekylgränssnittsmembran.
Vid emulgering av emulgeringskraven:
S: Emulgatoren måste kunna adsorbera eller berika gränssnittet mellan de två faserna, så att gränsytespänningen reduceras;
B: Emulgatoren måste ge partiklarna till laddningen, så att elektrostatisk avstötning mellan partiklarna eller bildar ett stabilt, mycket visköst skyddande membran runt partiklarna.
Därför måste ämnet som används som emulgator ha amfifiliska grupper för att emulgera, och ytaktiva medel kan uppfylla detta krav.
② Beredningsmetoder för emulsioner och faktorer som påverkar stabiliteten hos emulsioner
Det finns två sätt att förbereda emulsioner: en är att använda den mekaniska metoden för att sprida vätskan i små partiklar i en annan vätska, som mest används i industrin för att förbereda emulsioner; Den andra är att lösa vätskan i molekyltillstånd i en annan vätska och sedan få den att samlas ordentligt för att bilda emulsioner.
Stabiliteten hos en emulsion är förmågan att aggregera anti-partikel som leder till fasseparation. Emulsioner är termodynamiskt instabila system med stor fri energi. Därför är den så kallade stabiliteten hos en emulsion faktiskt den tid som krävs för att systemet ska nå jämvikt, dvs den tid som krävs för separering av en av vätskorna i systemet att inträffa.
När gränssnittsmembranet med fett alkoholer, fettsyror och fettaminer och andra polära organiska molekyler, är membranstyrkan betydligt högre. Detta beror på att, i det gränsytan adsorptionsskiktet av emulgieringsmolekyler och alkoholer, syror och aminer och andra polära molekyler för att bilda ett "komplex", så att gränsytemembranstyrkan ökade.
Emulgatorer som består av mer än två ytaktiva medel kallas blandade emulgatorer. Blandad emulgator adsorberad vid vatten/oljegränssnittet; Intermolekylär verkan kan bilda komplex. På grund av den starka intermolekylära verkan reduceras gränsytespänningen avsevärt, mängden emulgator som adsorberas vid gränssnittet ökas avsevärt, bildningen av gränsytmembrantensiteten ökar, styrkan ökar.
Laddningen för vätskepärlorna har en betydande effekt på stabiliteten hos emulsionen. Stabila emulsioner, vars flytande pärlor i allmänhet är laddade. När en jonisk emulgator används har emulgeringsjonen adsorberad vid gränssnittet sin lipofila grupp infört i oljefasen och den hydrofila gruppen är i vattenfasen, vilket gör att vätskepärlorna laddas. När emulsionspärlorna med samma laddning avvisar de varandra, inte lätt att agglomerat, så att stabiliteten ökas. Det kan ses att ju mer emulgerande joner adsorberade på pärlorna, desto större laddning, desto större är förmågan att förhindra pärlorna från agglomeration, desto stabilare är emulsionssystemet.
Viskositeten hos emulsionsdispersionsmediet har ett visst inflytande på stabiliteten hos emulsionen. Generellt sett, ju högre viskositeten hos dispersionsmediet, desto högre stabilitet hos emulsionen. Detta beror på att viskositeten hos dispersionsmediet är stor, vilket har en stark effekt på den browniska rörelsen hos vätskepärlorna och bromsar kollisionen mellan flytande pärlor, så att systemet förblir stabilt. Vanligtvis kan polymerämnen som kan lösas i emulsioner öka systemets viskositet och göra stabiliteten hos emulsioner högre. Dessutom kan polymerer också bilda ett starkt gränssnittsmembran, vilket gör emulsionssystemet mer stabilt.
I vissa fall kan tillsatsen av fast pulver också göra att emulsionen tenderar att stabilisera. Fast pulver är i vattnet, oljan eller gränssnittet, beroende på olja, vatten på vätningskapaciteten för det fasta pulvret, om det fasta pulvret inte är helt vått med vatten, utan också vått av olja, kommer att förbli på vatten- och oljegränssnittet.
Det fasta pulvret gör inte emulsionen stabilt eftersom pulvret som samlats vid gränssnittet förbättrar gränssnittsmembranet, som liknar det gränssnittet adsorption av emulgeringsmolekyler, så ju närmare det fasta pulvermaterialet är ordnat vid gränssnittet, desto stabilare är emulsionen.
Ytaktiva medel har förmågan att avsevärt öka lösligheten hos olösliga eller något vattenlösliga organiska ämnen efter bildning av miceller i vattenlösning, och lösningen är transparent för närvarande. Denna effekt av micellen kallas solubilisering. Den ytaktiva medel som kan producera solubilisering kallas solubilisator, och det organiska materialet som solubiliseras kallas solubiliserat material.

Skum spelar en viktig roll i tvättprocessen. Skum är ett dispersionssystem där en gas sprids i en vätska eller fast, med gasen som den spridda fasen och vätskan eller fast som det spridande mediet, den förstnämnda kallas flytande skum, medan det senare kallas fast skum, såsom skumlast, skumglas, skummed cement etc.
(1) Skumbildning
Med skum menar vi här ett aggregat av luftbubblor separerade med ett flytande membran. Denna typ av bubbla stiger alltid snabbt till vätskan på grund av den stora skillnaden i densitet mellan den spridda fasen (gas) och spridningsmediet (vätska), i kombination med vätskans låga viskositet.
Processen att bilda en bubbla är att föra en stor mängd gas i vätskan, och bubblorna i vätskan återgår snabbt till ytan och bildar ett aggregat bubblor separerade med en liten mängd flytande gas.
Skum har två betydande egenskaper när det gäller morfologi: en är att bubblorna som en spridd fas ofta är polyhedral i form, detta beror på att i skärningspunkten mellan bubblorna finns det en tendens att vätskefilmen tunnar så att bubblorna blir polyhedrala, när vätskefilmen minskar till en viss utsträckning leder det till bubblan. Den andra är att rena vätskor inte kan bilda stabilt skum, vätskan som kan bilda skum är minst två eller flera komponenter. Vattenlösningar av ytaktiva ämnen är typiska för system som är benägna att skumma generering, och deras förmåga att generera skum är också relaterad till andra egenskaper.
Ytaktiva medel med god skumningskraft kallas skummande medel. Även om skumningsmedlet har god skumförmåga, men skummet som bildas kanske inte kan upprätthålla lång tid, det vill säga dess stabilitet är inte nödvändigtvis bra. För att bibehålla skumets stabilitet, ofta i skumningsmedlet för att lägga till ämnen som kan öka stabiliteten hos skummet, kallas substansen skumstabilisator, vanligtvis används stabilisator lauryldietanolamin och dodekyldimetylaminoxid.
(2) skumets stabilitet
Skum är ett termodynamiskt instabilt system och den slutliga trenden är att vätskans totala ytarea i systemet minskar efter att bubblan har brutits och den fria energin minskar. Defoaming -processen är processen genom vilken vätskemembranet som skiljer gasen blir tjockare och tunnare tills den går sönder. Därför bestäms skumets stabilitetsgrad huvudsakligen av hastigheten på flytande urladdning och styrkan i vätskefilmen. Följande faktorer påverkar också detta.
(3) Skumförstörelse
Den grundläggande principen för skumförstörelse är att ändra förhållandena som producerar skummet eller att eliminera skumets stabiliserande faktorer, så det finns både fysiska och kemiska metoder för defoaming.
Fysisk defoaming innebär att ändra förhållandena för skumproduktion samtidigt som skumlösningens kemiska sammansättning, såsom yttre störningar, förändringar i temperatur eller tryck och ultraljudsbehandling är alla effektiva fysiska metoder för att eliminera skum.
Den kemiska avklädningsmetoden är att lägga till vissa ämnen för att interagera med skummedlet för att minska styrkan hos vätskefilmen i skummet och därmed minska skumets stabilitet för att uppnå syftet med defoaming, sådana ämnen kallas defoamers. De flesta av defoamers är ytaktiva ämnen. Därför, enligt mekanismen för defoaming, bör defoamer ha en stark förmåga att minska ytspänningen, lätt att adsorbera på ytan, och interaktionen mellan ytadsorptionsmolekylerna är svag, adsorptionsmolekyler arrangerade i en mer lossande struktur.
Det finns olika typer av defoamer, men i princip är de alla icke-joniska ytaktiva medel. Icke-joniska ytaktiva medel har anti-skumande egenskaper nära eller över deras molnpunkt och används ofta som defoamerer. Alkoholer, särskilt alkoholer med grenstruktur, fettsyror och fettsyrestrar, polyamider, fosfatestrar, silikonoljor, etc. används också vanligtvis som utmärkta defoamerer.
(4) Skum och tvätt
Det finns ingen direkt koppling mellan skum och tvätteffektivitet och mängden skum indikerar inte tvättens effektivitet. Till exempel har nonjoniska ytaktiva medel mycket färre skummande egenskaper än tvålar, men deras sanering är mycket bättre än tvålar.
I vissa fall kan skum vara till hjälp för att ta bort smuts och smuts. Till exempel, när man tvättar disk i hemmet, tar skummet på tvättmedlet upp oljedropparna och när du skrubber mattor hjälper skummet att plocka upp damm, pulver och annan fast smuts. Dessutom kan skum ibland användas som en indikation på effektiviteten hos ett tvättmedel. Eftersom fettoljor har en hämmande effekt på skummet i tvättmedlet, när det finns för mycket olja och för lite tvättmedel, kommer inget skum att genereras eller det ursprungliga skummet försvinner. Skum kan också ibland användas som en indikator på renheten hos en sköljning, eftersom mängden skum i sköljlösningen tenderar att minska med minskningen av detergentet, så mängden skum kan användas för att utvärdera sköljningsgraden.
I bred mening är tvätt processen att ta bort oönskade komponenter från det objekt som ska tvättas och uppnå något syfte. Tvätt i vanlig mening avser processen att ta bort smuts från bäraren. Vid tvätt försvagas eller elimineras interaktionen mellan smuts och bärare genom verkan av vissa kemiska ämnen (t.ex. tvättmedel, etc.), så att kombinationen av smuts och bärare ändras till kombinationen av smuts och tvättmedel, och slutligen separeras smuts från bäraren. Eftersom de föremål som ska tvättas och smuts som ska tas bort är olika, tvätt är en mycket komplex process och den grundläggande tvättprocessen kan uttryckas i följande enkla förhållanden.
Carrie ·· smuts + tvättmedel = bärare + smuts · tvättmedel
Tvättprocessen kan vanligtvis delas upp i två steg: för det första, under detergentets verkan, separeras smuts från dess bärare; För det andra sprids och suspenderas den fristående smuts i mediet. Tvättprocessen är en reversibel process och smuts spridd och suspenderad i mediet kan också återutfällas från mediet till objektet tvättas. Därför bör ett bra tvättmedel ha förmågan att sprida och stänga smuts och förhindra omposition av smuts, utöver förmågan att ta bort smuts från bäraren.
(1) typer av smuts
Även för samma objekt kan typen, sammansättningen och mängden smuts variera beroende på miljön där den används. Oljekroppsmutt är främst några djur- och vegetabiliska oljor och mineraloljor (såsom råolja, eldningsolja, koltjära, etc.), fast smuts är främst sot, aska, rost, kolsvart, etc. När det gäller kläder smuts, finns det smuts från människokroppen, såsom svett, talg, blod, etc .; Smuts från mat, såsom fruktfläckar, matlagningsfläckar, smaktalfläckar, stärkelse osv.; smuts från kosmetika, såsom läppstift, nagellack, etc.; smuts från atmosfären, såsom sot, damm, lera osv.; Andra, såsom bläck, te, beläggning, etc. Det finns i olika typer.
De olika typerna av smuts kan vanligtvis delas upp i tre huvudkategorier: fast smuts, flytande smuts och special smuts.
① Fast smuts
Vanlig fast smuts inkluderar partiklar av aska, lera, jord, rost och kolsvart. De flesta av dessa partiklar har en elektrisk laddning på ytan, de flesta av dem är negativt laddade och kan lätt adsorberas på fiberartiklar. Fast smuts är i allmänhet svårt att lösa upp i vatten, men kan spridas och suspenderas av tvättmedelslösningar. Fast smuts med mindre masspunkt är svårare att ta bort.
② flytande smuts
Flytande smuts är mestadels oljelöslig, inklusive växt- och animaliska oljor, fettsyror, fettalkoholer, mineraloljor och deras oxider. Bland dem kan växt- och animaliska oljor, fettsyror och alkali -förtvålning förekomma, medan fett alkoholer, mineraloljor inte är förtväckande av alkali, utan kan vara lösliga i alkoholer, etrar och kolväte organiska lösningsmedel och detergent vattenlösningsemulering och spridning. Oljelöslig vätska smuts har i allmänhet en stark kraft med fiberartiklar och är mer fast adsorberad på fibrer.
③ Special smuts
Speciellt smuts inkluderar proteiner, stärkelse, blod, mänskliga utsöndringar som svett, talg, urin och fruktjuice och tesaft. Det mesta av denna typ av smuts kan vara kemiskt och starkt adsorberade på fiberartiklar. Därför är det svårt att tvätta.
De olika typerna av smuts finns sällan ensamma, men blandas ofta och adsorberas på föremålet. Smuts kan ibland oxideras, sönderdelas eller förfallas under yttre påverkan, vilket skapar ny smuts.
(2) vidhäftning av smuts
Kläder, händer etc. kan färgas eftersom det finns någon form av interaktion mellan föremålet och smuts. Smuts följer föremål på olika sätt, men det finns inte mer än fysiska och kemiska vidhäftningar.
① Vidhäftningen av sot, damm, lera, sand och kol till kläder är en fysisk vidhäftning. Generellt sett, genom denna vidhäftning av smuts, och rollen mellan det färgade föremålet är relativt svag, är borttagningen av smuts också relativt enkelt. Enligt de olika krafterna kan den fysiska vidhäftningen av smuts delas upp i mekanisk vidhäftning och elektrostatisk vidhäftning.
A: Mekanisk vidhäftning
Denna typ av vidhäftning hänvisar huvudsakligen till vidhäftningen av någon fast smuts (t.ex. damm, lera och sand). Mekanisk vidhäftning är en av de svagare formerna av vidhäftning av smuts och kan tas bort nästan med rent mekaniska medel, men när smuts är liten (<0,1um) är det svårare att ta bort.
B : Elektrostatisk vidhäftning
Elektrostatisk vidhäftning manifesteras huvudsakligen i verkan av laddade smutspartiklar på motsatt laddade föremål. De flesta fibrösa föremål är negativt laddade i vatten och kan lätt följas av vissa positivt laddade smuts, såsom kalktyper. En del smuts, även om de är negativt laddade, såsom kolsvartpartiklar i vattenhaltiga lösningar, kan följa fibrer genom jonbroar (joner mellan flera motsatt laddade föremål, agerar tillsammans med dem på ett broliknande sätt) bildade av positiva joner i vatten (t.ex. Ca2+ , Mg2+ etc.).
Elektrostatisk verkan är starkare än enkel mekanisk verkan, vilket gör att smuts avlägsnar relativt svårt.
② Kemisk vidhäftning
Kemisk vidhäftning avser fenomenet smuts som verkar på ett föremål genom kemiska eller vätebindningar. Till exempel, polärt fasta smuts, protein, rost och annan vidhäftning på fiberartiklar, fibrer innehåller karboxyl, hydroxyl, amid och andra grupper, dessa grupper och oljiga smutsfettsyror, fetthaltiga alkoholer är enkla att bilda vätebindningar. De kemiska krafterna är i allmänhet starka och smuts är därför mer fast bundna till föremålet. Denna typ av smuts är svår att ta bort med de vanliga metoderna och kräver speciella metoder för att hantera det.
Graden av vidhäftning av smuts är relaterad till själva smutsens natur och arten av det objekt som den följs för. Generellt följer partiklar lätt till fibrösa föremål. Ju mindre strukturen på den fasta smuts, desto starkare vidhäftningen. Polar smuts på hydrofila föremål som bomull och glas fäster starkare än icke-polär smuts. Icke-polär smuts följer starkare än polär smuts, såsom polära fetter, damm och lera, och är mindre lätt att ta bort och rengöra.
(3) Mekanism för smuts borttagning
Syftet med tvätt är att ta bort smuts. I ett medium av en viss temperatur (huvudsakligen vatten). Med användning av de olika fysiska och kemiska effekterna av tvättmedlet för att försvaga eller eliminera effekten av smuts och tvättade föremål, under verkan av vissa mekaniska krafter (såsom handgubbning, tvättmaskinens agitation, vattenpåverkan), så att smuts och tvättade föremål från syftet med dekontaminering.
① Mekanism för flytande smuts borttagning
En : Vätning
Flytande smuts är mestadels oljebaserad. Oljefläckar våta de flesta fibrösa föremål och sprids mer eller mindre som en oljefilm på ytan av fibrösa material. Det första steget i tvättverkan är vätningen av ytan av tvättvätskan. För illustrationens skull kan ytan på en fiber betraktas som en slät fast yta.
B: oljeavskiljning - curlingmekanism
Det andra steget i tvättverkan är avlägsnande av olja och fett, avlägsnande av flytande smuts uppnås genom en slags spolning. Vätskan smuts fanns ursprungligen på ytan i form av en spridd oljefilm, och under den förmånliga vätningseffekten av tvättvätskan på den fasta ytan (dvs. fiberytan) krullade den upp i oljepärlor steg för steg, som ersattes av tvättvätskan och lämnade så småningom ytan under vissa yttre krafter.
② Mekanism för borttagning av fasta smuts
Avlägsnande av flytande smuts är huvudsakligen genom den förmånliga vätningen av smutsbären genom tvättlösningen, medan borttagningsmekanismen för fast smuts är annorlunda, där tvättprocessen huvudsakligen handlar om vätningen av smutsmassan och dess bäraryta vid tvättlösningen. På grund av adsorptionen av ytaktiva ämnen på den fasta smuts och dess bäraryta, reduceras interaktionen mellan smuts och ytan och vidhäftningsstyrkan hos smutsmassan på ytan reduceras, så smutsmassan avlägsnas lätt från bäraren.
Dessutom har adsorptionen av ytaktiva medel, särskilt joniska ytaktiva medel, på ytan av den fasta smuts och dess bärare potential att öka ytpotentialen på ytan av den fasta smuts och dess bärare, vilket är mer gynnsamt för att ta bort smuts. Fasta eller generellt fibrösa ytor laddas vanligtvis negativt i vattenhaltiga medier och kan därför bilda diffusa dubbla elektroniska skikt på smutsmassor eller fasta ytor. På grund av avstötning av homogena laddningar försvagas vidhäftningen av smutspartiklar i vattnet till den fasta ytan. När ett anjoniskt ytaktivt medel tillsätts, eftersom det samtidigt kan öka den negativa ytpotentialen hos smutspartikeln och den fasta ytan, är avvisningen mellan dem mer förbättrad, vidhäftningsstyrkan hos partikeln är mer reducerad och smuts är lättare att ta bort.
Icke-joniska ytaktiva ämnen adsorberas på generellt laddade fasta ytor och även om de inte väsentligt förändrar gränsytepotentialen, tenderar de adsorberade icke-joniska ytaktiva ämnen att bilda en viss tjocklek av adsorberat skikt på ytan som hjälper till att förhindra att rundeposition av smuts.
När det gäller katjoniska ytaktiva medel minskar eller eliminerar deras adsorption den negativa ytpotentialen hos smutsmassan och dess bäraryta, vilket minskar avvisningen mellan smuts och ytan och är därför inte gynnsam till smutsavlägsnande; Vidare, efter adsorption på den fasta ytan, tenderar katjoniska ytaktiva ämnen att vända den fasta ytan hydrofob och är därför inte gynnsamma för ytvätning och därför tvätt.
③ Avlägsnande av speciella jordar
Protein, stärkelse, mänskliga sekret, fruktjuice, tesaft och annan sådan smuts är svåra att ta bort med normala ytaktiva medel och kräver speciell behandling.
Proteinfläckar som grädde, ägg, blod, mjölk och hudutsöndring tenderar att koagulera på fibrerna och degenerationen och få starkare vidhäftning. Proteinsling kan tas bort med hjälp av proteaser. Enzymet proteas bryter ner proteinerna i smuts i vattenlösliga aminosyror eller oligopeptider.
Stärkelsefläckar kommer främst från livsmedel, andra som sås, lim etc. Amylas har en katalytisk effekt på hydrolysen av stärkelsefläckar, vilket får stärkelse att bryta ner i sockerarter.
Lipas katalyserar nedbrytningen av triglycerider, som är svåra att ta bort med normala metoder, såsom talg- och ätliga oljor, och bryter ner dem till löslig glycerol och fettsyror.
Vissa färgade fläckar från fruktjuicer, tesaft, bläck, läppstift etc. är ofta svåra att rengöra noggrant även efter upprepad tvätt. Dessa fläckar kan avlägsnas genom en redoxreaktion med ett oxidations- eller reducerande medel såsom blekmedel, vilket förstör strukturen för färggenererande eller färg auxiliary-grupper och försämrar dem till mindre vattenlösliga komponenter.
(4) fläckborttagningsmekanism för kemtvätt
Ovanstående är faktiskt för vatten som tvättmedium. I själva verket, på grund av de olika typerna av kläder och struktur, är vissa kläder som använder vattentvätt inte bekvämt eller inte lätt att tvätta rena, vissa kläder efter tvätt och till och med deformation, blekning, etc., till exempel: De flesta naturliga fibrer absorberar vatten och lätt att svälla och torka och lätt att krympa, så efter tvätt kommer att deformeras; Genom att tvätta ullprodukter verkar också ofta krympningsfenomen, är vissa ullprodukter med vattentvätt också lätt att pilla, färgförändring; Vissa silkes handkänsla blir sämre efter tvätt och tappat sin lyster. För dessa kläder använder ofta torrrengöringsmetoden för att dekontaminera. Den så kallade kemtvätten hänvisar i allmänhet till tvättmetoden i organiska lösningsmedel, särskilt i icke-polära lösningsmedel.
Krematrengöring är en mildare form av tvätt än vattentvätt. Eftersom kemtvätt inte kräver mycket mekanisk verkan orsakar det inte skador, rynkor och deformation till kläder, medan kemtvättmedel, till skillnad från vatten, sällan ger expansion och sammandragning. Så länge tekniken hanteras ordentligt kan kläderna torka utan distorsion, färgblekning och förlängd livslängd.
När det gäller kemtvätt finns det tre breda typer av smuts.
① Ojolös smutsoljelöslig smuts inkluderar alla typer av olja och fett, som är flytande eller fet och kan lösas i kemtvättlösningsmedel.
② Vattenlösligt smuts vattenlösligt smuts är lösliga i vattenhaltiga lösningar, men inte i kemtvättmedel, adsorberas på kläder i vattenhaltigt tillstånd, vatten avdunstar efter utfällningen av granulära fasta ämnen, såsom oorganiska salter, stärkelse, protein, etc.
③ Olja och vattenolöslig smutsolja och vattenolöslig smuts är varken löslig i vatten eller lösliga i kemtvättlösningsmedel, såsom kolsvart, silikater av olika metaller och oxider, etc.
På grund av olika karaktärer av olika typer av smuts finns det olika sätt att ta bort smuts i torrrengöringsprocessen. Oljelösliga jordar, såsom djur- och vegetabiliska oljor, mineraloljor och fett, är lätt lösliga i organiska lösningsmedel och kan lättare tas bort vid kemtvätt. Den utmärkta lösligheten av kemtvättlösningsmedel för oljor och fett kommer i huvudsak från Van der väggkrafter mellan molekyler.
För avlägsnande av vattenlöslig smuts såsom oorganiska salter, sockerarter, proteiner och svett, måste den rätta mängden vatten också läggas till torrrengöringsmedel, annars är vattenlöslig smuts svårt att ta bort från kläderna. Vatten är emellertid svårt att lösa upp i kemtvättmedlet, så för att öka mängden vatten måste du också lägga till ytaktiva ämnen. Närvaron av vatten i torrrengöringsmedel kan göra ytan på smuts och kläder hydratiserad, så att det är lätt att interagera med de polära grupperna av ytaktiva medel, vilket bidrar till adsorptionen av ytaktiva medel på ytan. Dessutom, när ytaktiva medel bildar miceller, kan vattenlöslig smuts och vatten solubiliseras i micellerna. Förutom att öka vatteninnehållet i det torra rengörande lösningsmedlet, kan ytaktiva ämnen också spela en roll för att förhindra återinställning av smuts för att förbättra saneringseffekten.
Närvaron av en liten mängd vatten är nödvändig för att avlägsna vattenlöslig smuts, men för mycket vatten kan orsaka snedvridning och rynkor i vissa kläder, så mängden vatten i kemtvättmedlet måste vara måttligt.
Smuts som varken är vattenlöslig eller oljelöslig, fasta partiklar som aska, lera, jord och kolsvart, är vanligtvis fäst vid plagget av elektrostatiska krafter eller i kombination med olja. In dry cleaning, the flow of solvent, impact can make the electrostatic force adsorption of dirt off, and dry-cleaning agent can dissolve the oil, so that the combination of oil and dirt and attached to the clothing of solid particles off in the dry-cleaning agent, dry cleaning agent in a small amount of water and surfactants, so that those off the solid dirt particles can be stable suspension, dispersion, to prevent its re-deposition to the kläder.
(5) Faktorer som påverkar tvättåtgärder
Riktningsadsorptionen av ytaktiva medel vid gränssnittet och minskningen av ytan (gränsytespänningen är de viktigaste faktorerna vid avlägsnande av vätska eller fast smuts. Tvättprocessen är emellertid komplex och tvätteffekten, även med samma tvättmedelstyp, påverkas av många andra faktorer. Dessa faktorer inkluderar koncentrationen av tvättmedlet, temperaturen, arten av smuts, typen av fiber och strukturen på tyget.
① Surfaktantkoncentration
Micellerna av ytaktiva medel i lösningen spelar en viktig roll i tvättprocessen. När koncentrationen når den kritiska micellkoncentrationen (CMC) ökar tvätteffekten kraftigt. Därför bör koncentrationen av tvättmedel i lösningsmedlet vara högre än CMC -värdet för att ha en god tvätteffekt. Men när koncentrationen av ytaktivt medel är högre än CMC -värdet är den inkrementella ökningen i tvätteffekten inte uppenbar och det är inte nödvändigt att öka koncentrationen av ytaktivt medel för mycket.
Vid avlägsnande av olja genom solubilisering ökar solubiliseringseffekten med ökande ytaktivkoncentration, även när koncentrationen är över CMC. För närvarande är det tillrådligt att använda tvättmedel på ett lokalt centraliserat sätt. Om det till exempel finns mycket smuts på manschetten och kragen i ett plagg, kan ett skikt av tvättmedel appliceras under tvätt för att öka den solubiliserande effekten av det ytaktiva ämnet på oljan.
②temperatur har ett mycket viktigt inflytande på saneringsåtgärden. I allmänhet underlättar temperaturen avlägsnande av smuts, men ibland kan en för hög temperatur också orsaka nackdelar.
Ökningen i temperatur underlättar diffusionen av smuts, fast fett emulgeras lätt vid temperaturer över dess smältpunkt och fibrerna ökar i svullnad på grund av ökningen i temperaturen, som alla underlättar avlägsnande av smuts. För kompakta tyger reduceras emellertid mikrogerna mellan fibrerna när fibrerna expanderar, vilket är skadligt för avlägsnande av smuts.
Temperaturförändringar påverkar också lösligheten, CMC -värdet och micellstorleken på ytaktiva ämnen, vilket påverkar tvätteffekten. Lösligheten hos ytaktiva medel med långa kolkedjor är låg vid låga temperaturer och ibland är lösligheten ännu lägre än CMC -värdet, så tvätttemperaturen bör höjas på lämpligt sätt. Effekten av temperatur på CMC-värdet och micellstorleken är annorlunda för joniska och icke-joniska ytaktiva medel. För joniska ytaktiva medel ökar en ökning av temperaturen i allmänhet CMC -värdet och minskar micellstorleken, vilket innebär att koncentrationen av ytaktivt medel i tvättlösningen bör ökas. För icke-joniska ytaktiva medel leder en ökning av temperaturen till en minskning av CMC-värdet och en signifikant ökning av micellvolymen, så det är tydligt att en lämplig temperaturökning kommer att hjälpa det icke-joniska ytaktiva medel att utöva sin ytaktiva effekt. Temperaturen bör dock inte överstiga molnpunkten.
Kort sagt beror den optimala tvätttemperaturen på tvättmedelsformuleringen och objektet tvättas. Vissa tvättmedel har en god tvättmedelseffekt vid rumstemperatur, medan andra har en mycket annorlunda tvättstagare mellan kall och varm tvätt.
③ skum
Det är vanligt att förvirra skumningskraft med tvätteffekt och tror att tvättmedel med hög skummande kraft har en god tvätteffekt. Forskning har visat att det inte finns något direkt samband mellan tvätteffekten och mängden skum. Till exempel är tvätt med låga skummande tvättmedel inte mindre effektivt än tvätt med höga skummande tvättmedel.
Även om skum inte är direkt relaterat till tvätt, finns det tillfällen när det hjälper till att ta bort smuts, till exempel när du tvättar disk för hand. När skurvarpets kan skum också ta bort damm och andra fasta smutspartiklar, mattar smuts står för en stor del av damm, så mattrengöringsmedel bör ha en viss skumförmåga.
Skumkraft är också viktigt för schampon, där det fina skummet som produceras av vätskan under schamponering eller badning gör att håret känner sig smörjat och bekvämt.
④ Varianter av fibrer och fysiska egenskaper hos textilier
Förutom den kemiska strukturen hos fibrerna, som påverkar vidhäftningen och avlägsnande av smuts, har fibrernas utseende och organisationen av garnet och tyget påverkat lättheten att avlägsna smuts.
Vågen av ullfibrer och de böjda platta band av bomullsfibrer är mer benägna att samla smuts än släta fibrer. Till exempel är kolsvart färgad på cellulosafilmer (viskosfilmer) lätt att ta bort, medan kolsvart färgade på bomullstyg är svårt att tvätta av. Ett annat exempel är att kortfibertyg som är gjorda av polyester är mer benägna att ackumulera oljefläckar än långfibertyger, och oljefläckar på kortfibertyg är också svårare att ta bort än oljefläckar på långfibertyger.
Tätt vridna garn och snäva tyger, på grund av det lilla gapet mellan fibrerna, kan motstå invasionen av smuts, men detsamma kan också förhindra att tvättvätskan utesluter de inre smuts, så snäva tyger börjar motstå smuts bra, men när färgad tvätt är också svårare.
⑤ Vattenhårdhet
Koncentrationen av Ca2+, Mg2+ och andra metalljoner i vattnet har ett stort inflytande på tvätteffekten, särskilt när de anjoniska ytaktiva ämnena möter Ca2+ och Mg2+ -joner som bildar kalcium och magnesiumsalter som är mindre lösliga och kommer att minska dess detergens. I hårt vatten, även om koncentrationen av ytaktivt medel är hög, är tvättstugan fortfarande mycket värre än vid destillation. För att ytaktivmedlet ska ha den bästa tvätteffekten, bör koncentrationen av Ca2+ -joner i vattnet reduceras till 1 x 10-6 mol/L (Caco3 till 0,1 mg/L) eller mindre. Detta kräver tillägg av olika mjukgörare till tvättmedlet.
Posttid: feb-25-2022



